医药生物行业及资本市场周报(2018年11月5日~11月11日)
(一)大盘及行业指数走势
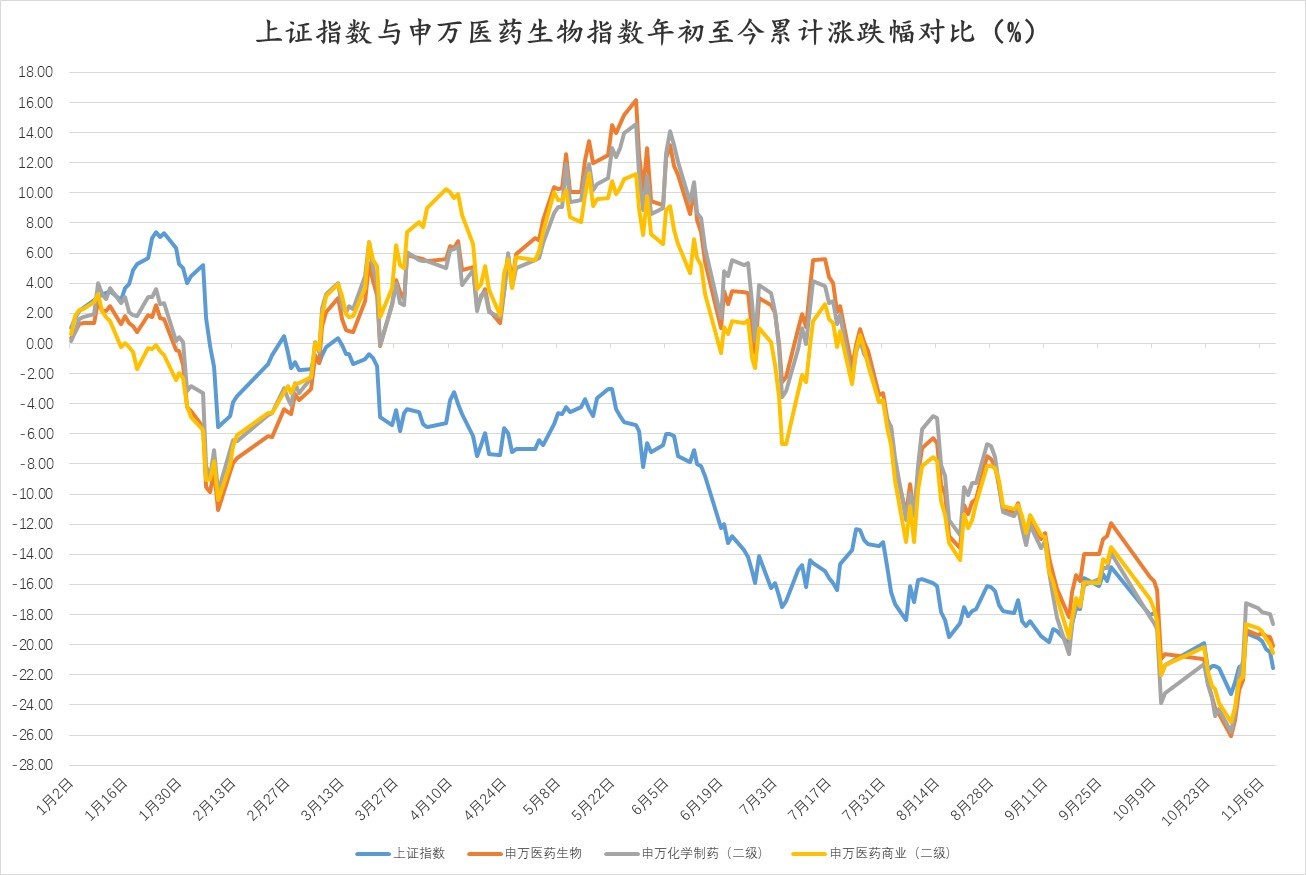
下表列示了本周大盘指数每日涨跌幅情况,并附上月初和年初至今累计涨跌幅数据,供参考:
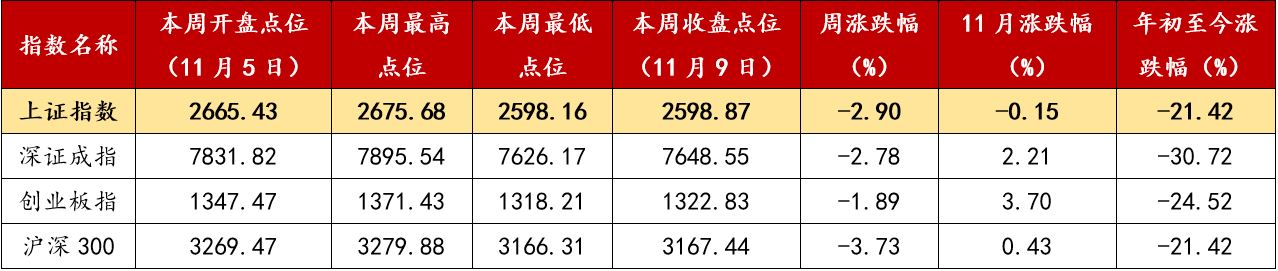
作为对照,下表列示了申万医药行业(一级)指数以及下面六大子行业指数同期的涨跌幅情况:
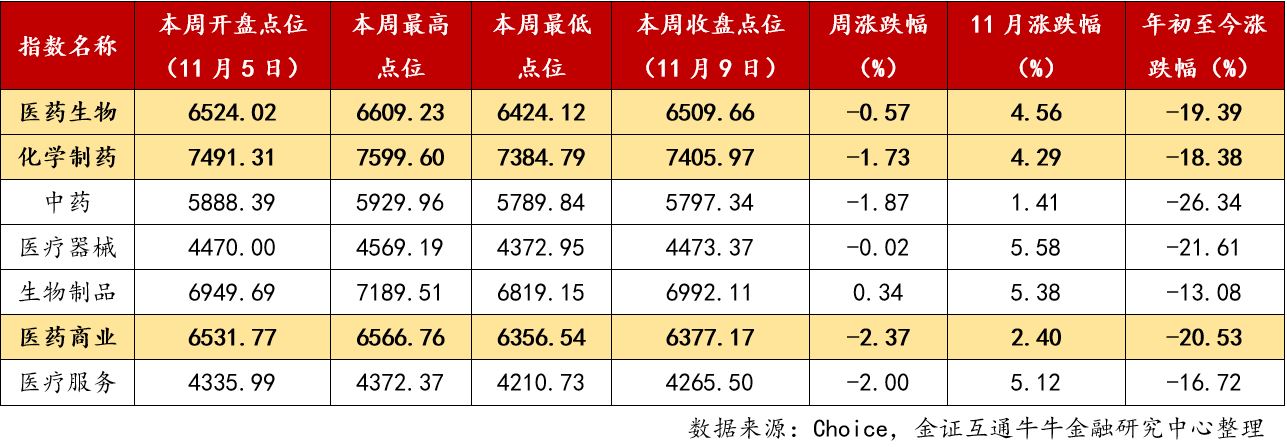
金证简评:大盘阴跌行业涨幅回吐,但不改长期趋势。截至本周五,上证综指本周下跌近3%,2600整数关口得而复失,报2598.87点,深证成指和创业板指涨幅分别收跌2.78%和1.89%,报7648.55和1322.83点。医药生物板块本周在进博会和基药目录等正面事件的护盘作用下窄幅震荡,申万医药生物行业指数本周微跌0.57%,报6509.66点,跌幅少于沪指2.33个百分点,少于深指和创业板指2.21和1.32个百分点。
板块估值方面,截至周五盘后A股全市场市盈率(TTM)微降至11.64倍,而医药生物板块为28.78倍,估值溢价率小幅升至147.24%。各子行业估值涨跌不一,分板块具体数据为:化药28.55倍,中药19.85倍,生物制品49.56倍,医药商业18.40倍,医疗器械36.55倍,医疗服务74.29倍。
本周大盘整体下行,医药相对大盘下跌较少。2018年前三季度,受行业政策波动以及宏观经济下行的压力增大的影响,一方面行业带量采购试点、医保支付谈判结果、基药目录发布等政策结果逐步落地;另一方面,“两票制”影响下药企“低开转高开”产生的费用将逐步在三季度和四季度释放,业绩将逐步“消肿”。不过在长期负面情绪压制下,医药板块目前估值处于历史相对较低位置,随着市场情绪逐步的回归理性,医药板块也有望迎来超跌后的反弹机会。长期来看,具备创新能力,规范程度更高的龙头企业发展长期价值未发生太大变化,未来有望成为行情复苏时反弹的先锋和主力。
(二)监管与行业政策动态
1. 《疫苗管理法》今起征求意见,疫苗产销用环节全程监管从重处罚
11月11日晚间,国家市场监督管理总局网站发布了关于就《中华人民共和国疫苗管理法(征求意见稿)》(下称“征求意见稿”)公开征求意见的公告,征集公众意见至11月25日截止。
征求意见稿突出强调了疫苗战略性、公益性的性质与地位,在立法目的中明确提出维护国家安全的目的,同时也对疫苗生产流通全流程也都进行了明确规定。征求意见稿全文共十一章,对疫苗研制和上市许可、生产、上市后管理、流通、预防接种、异常反应监测、保障措施、监管和法律责任等方面都有针对性、实效性和可操作性的法律条款。并且,对于违法行为的处罚上,征求意见稿加大了处罚力度。
征求意见稿提出,国家对疫苗生产企业实行严于一般药品生产企业的准入制度。从事疫苗生产活动,应当经省、自治区、直辖市药品监督管理部门批准。准入从严的同时,对于疫苗生产过程,也强调了要实时记录。而在疫苗出厂后的批签发环节,征求意见稿要求疫苗产品在每批上市销售前,应当经国务院药品监督管理部门授权的药品检验机构按照相关技术要求进行审核、检验。符合要求的,发给生物制品批签发证明;不符合要求的,发给不予批签发通知书。值得注意的是,征求意见稿提出,国家实行疫苗责任强制保险制度。疫苗上市许可持有人应当购买责任保险。疫苗出现质量问题的,保险公司在承保责任范围内予以赔付。
根据征求意见稿,疫苗上市许可持有人应当建立健全疫苗质量管理体系,制定并实施疫苗上市后风险管理计划,主动开展疫苗上市后研究,对疫苗的安全性、有效性进行进一步确证。必要时,国务院药品监督管理部门可以责令疫苗上市许可持有人开展上市后评价或者直接组织开展上市后评价。这也要求疫苗上市许可持有人应当对上市的疫苗进行质量跟踪分析,持续优化生产工艺和质量控制标准,提高工艺稳定性,及时变更制造和检定规程。
疫苗上市后研究管理也意味着,达不到要求的疫苗产品将面临退市和淘汰。征求意见稿提出,对于同品种疫苗中生产工艺落后、质量控制水平明显劣于其他同品种疫苗现有水平的,国务院药品监督管理部门责令疫苗上市许可持有人限期进行工艺优化和质量提升。在规定期限内仍达不到要求的,疫苗上市许可持有人应当主动申请注销疫苗的上市许可证明文件。未主动申请注销的,国务院药品监督管理部门撤销疫苗的上市许可证明文件。并且,国务院药品监督管理部门可以根据疾病预防控制需要和疫苗行业技术发展情况,组织对疫苗品种开展上市后评价,发现该类疫苗的产品设计、生产工艺、风险获益比明显劣于预防同种疾病的其他类疫苗的,撤销该类品种的所有上市许可证明文件及相应国家药品标准。
受长生生物疫苗事件的影响,本次征求意见稿大幅度提高了对疫苗违法违规事件的处罚力度。根据征求意见稿第89条,疫苗上市许可持有人有下列情形之一的,没收违法所得,责令停产停业,撤销上市许可证明文件,并处货值金额5倍以上10倍以下罚款;货值金额不足50万元的则处以100万元以上500万元以下罚款,对疫苗上市许可持有人的法定代表人、主要负责人和关键岗位人员,没收其在违法期间自本单位所获收入,并处50%以上、1倍以下罚款,10年内不得从事药品生产经营活动:
(1)提交虚假临床试验或者上市许可申报资料的;
(2)编造生产检定记录、更改产品批号的;
(3)提交虚假批签发申报资料,或者采取其他欺骗手段获得批签发证明的;
(4)发现上市销售的疫苗存在质量问题或者其他安全隐患,未采取召回措施的;
(5)其他具有主观故意的严重违法行为的。
上述情形特别严重的,吊销疫苗企业的药品生产许可证,其法定代表人、主要负责人和其他关键岗位人员终身不得从事药品生产经营活动。
2. 证监会:对4宗内幕交易案件作出行政处罚
在11月9日的例行新闻发布会上,证监会通报了对4宗违法违规案件的处罚决定:
(1)对冀晓斌内幕交易“延长化建”案作出处罚,没收违法所得3.28万元,并处罚金9.85万元;
(2)对潘广明内幕交易“宝泰隆”案作出处罚,没收违法所得2.66万元,并处罚金3万元;
(3)黑龙江证监局对姜亮亮内幕交易“宝泰隆”案作出处罚,对姜亮亮处以3万元罚款;
(4)广东证监局对陈磊内幕交易“保龄宝”案作出处罚,对陈磊处以3万元罚款。
证监会认定,上述案件中,冀晓斌在“延长化建重组北京工程公司”内幕信息敏感期内,在与内幕信息知情人联络接触后于次日异常交易了“延长化建”股票;姜亮亮、潘广明系“宝泰隆2017年股票激励计划”这一内幕信息的知情人,在内幕信息敏感期内,二人分别内幕交易了“宝泰隆”股票;陈磊配偶郑某林是“保龄宝相关股权转让事宜”的内幕信息知情人,在内幕信息敏感期内,陈磊利用与郑某林共同生活便利及频繁联络接触获悉了内幕信息,并内幕交易了“保龄宝”股票。
3. 药审中心正式启动药品临床实验默示许可制度,新药审评审批将再度提速
11月5日夜间,国家食药监总局药品审评中心官网显著位置,用红色显眼的标签更新了一个重要板块“临床试验默示许可公示”,这标志着中国的新药临床试验行政许可,由从前的“点头制”批准正式转入更加高效的“摇头制”批准时代。本次共公布首批默许共有8个受理号5个品种,其中不但有大型的外资制药企业品种,也有CX开头的创新类国产新药,见下图:
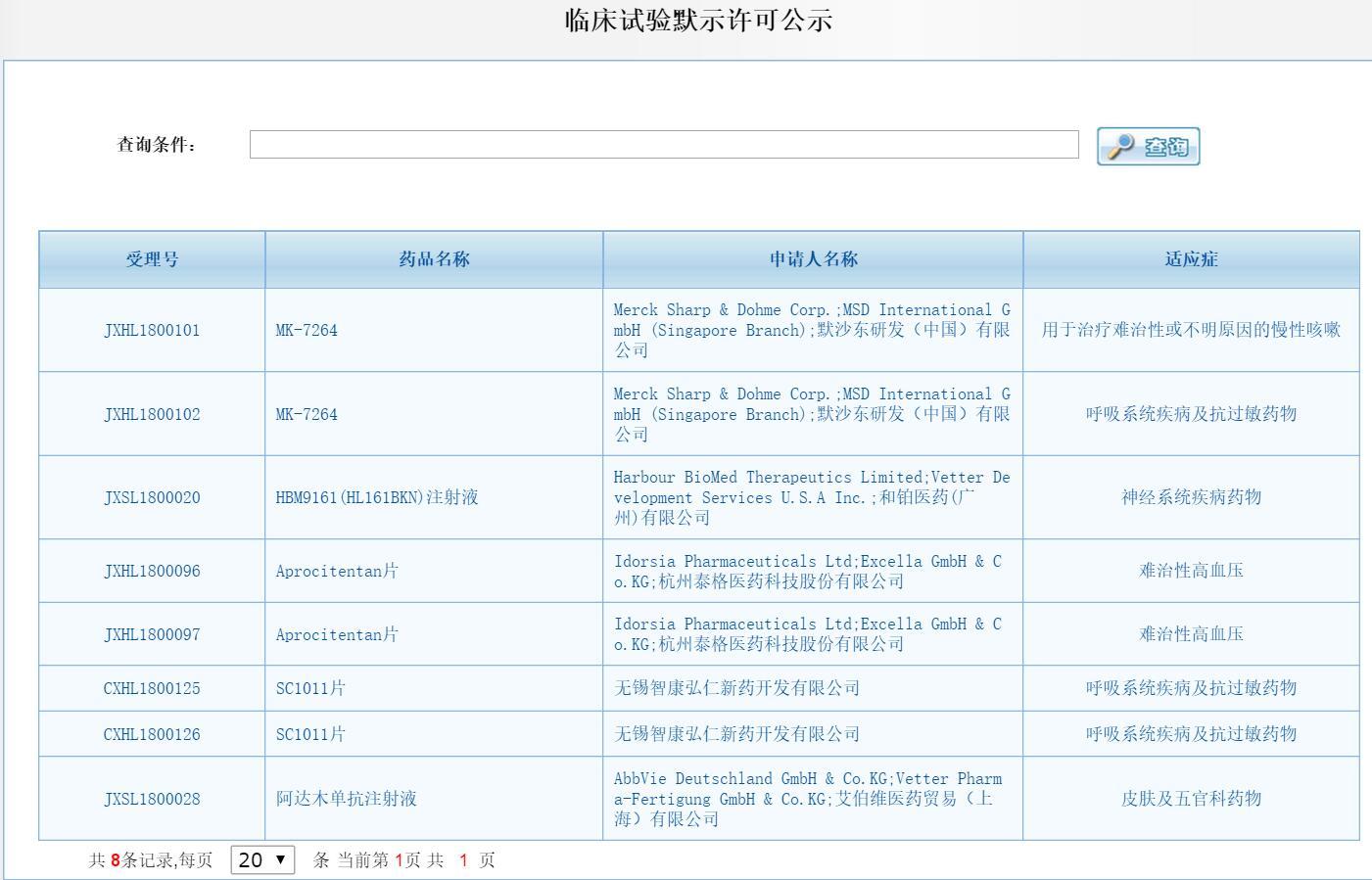
“将临床试验申请由批准制改为到期默认制,是国家药监部门一直努力的方向,政策是有延续性的,也并不突然。”一位参与药品审批的专家表示。医药界关于临床试验申请的审批制度改革的呼声一直不断,因为药物、器械产品更新迭代的速度非常快,而我国审批的过程较长,往往国外的第二代新药已经出现,第一代还没有进入中国,制约了医疗器械研发的进展,也使患者不能及时获益。
2015年8月,国务院发布《关于改革药品医疗器械审评审批制度的意见》,标志着临床试验申请审评审批流程优化工作开展,虽然在《意见》明确提出了 “解决注册申请积压”的目标和 “改进药品临床试验审批”的主要任务作为改革的大方向,但并未具体提及临床试验申请由批准制改为到期默认制。
2017年10月8日,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,这是对上述2015年《意见》的进一步深化,力度之大,引起业界广泛关注。在该文件中还首次提出了 “受理临床试验申请后一定期限内,食品药品监管部门未给出否定或质疑意见即视为同意,注册申请人可按照提交的方案开展临床试验”。
2017年12月11日,原食品药品监管总局发布了《关于调整药物临床试验审评审批的公告(征求意见稿)》。在该文件中提出的具体改革措施包括 “5日内完成形式审查” 、 “符合申报要求的发出受理通知自自受理之日起60日内,未收到药审中心否定或质疑意见的,申请人可以按照提交的方案开展临床试验”等 。这与过去一年多的等待时间相比,大大缩短了新药研发进程。同时,这也是国家药监机构第一次以征求意见稿的形式向外界发出临床试验申请改革的具体措施。
从正在进行默示许可公示的药品中可以看出,不仅有默沙东研发(中国)有限公司和艾伯维医药贸易(上海)有限公司等跨国药企的注册申请,也有来自和铂医药等国内创新药企业的申请。其中和铂医药的HBM9161(HL161BKN)注射液更有一款用于罕见病重症肌无力的药。
重症肌无力的患病率为77~150/100万,年发病率为4~11/100万。女性患病率大于男性,约3:2,各年龄段均有发病,儿童1~5岁居多。2018年5月,国家卫生健康委员会、科技部、工业和信息化部、国家药品监督管理局、国家中医药管理局等五部门联合发布的《第一批罕见病目录》,重症肌无力被列入其中。该病是临床上公认的难治疾病,预后差,进展快,同时也被全球大多数国家认定为罕见病。
4. 沪深交易所:本周监管措施执行情况
(1)上交所(5家)
红星美凯龙(601828):公司副总经理6个月内反复买入卖出公司股票,卖出行为构成减持但未事先公告,同时违反了“上市公司高级管理人员不得在公司股票上市之日起1年内转让”及“任职期间每年转让股份不超过本人所持有公司股份25%”的规定,给予通报批评处分,并通报中国证监会,记入上市公司诚信档案;
方正科技(600601):就公司治理等相关事项下发监管工作函(函件全文未公开);
诺力股份(603611):公司控股股东与一致行动人多次质押所持有公司股份未知会上市公司,给予通报批评处分,并通报中国证监会,记入上市公司诚信档案;
*ST抚钢(600399):公司未能在4月27日的规定期限内披露定期报告,直至2018年6月26日才予以披露,季报的行为影响投资者全面获取上市公司年度和季度信息的合理预期,严重损害投资者的知情权,造成了不良市场影响,对上市公司及董事长、董秘、董事(含独立董事)、监事等予以公开谴责,通报中国证监会和辽宁省人民政府,并将记入上市公司诚信档案;
时代万恒(600241):关联方万恒集团延期履行还款承诺,形成关联方非经营性资金占用,而但公司未就上述事项履行信息披露义务,也未就万恒集团后续还款进展等予以披露。对上市公司及关联方、董事长和财务总监、董秘予以公开批评。
(2)深交所(13家,因篇幅所限仅列示部分)
普利制药(300630):公司使用自有资金购买私募投资基金份额共计4000万元,但未履行相应的审议程序和信息披露义务;
尔康制药(300267):会计师事务所签字注册会计师未能勤勉尽责,出具的审计报告存在虚假记载;
星源材质(300568):独立董事离职后前往关联方继续担任独立董事,未告知上市公司;
坚瑞沃能(300116):公司今年上半年收到并确认政府补助12482.14万元,但直至11月7日方才在回复交易所问询函中披露各项补贴(助)明细。
(三)行业及同业公司动态
1. 尔康制药造假案后续:签字会计师收监管函,审计机构恐将成为追加被告
11月7日,深交所向天健会计师事务所胡萍发出监管函:作为尔康制药(300267.SZ)财务报告审计机构签字会计师,未能勤勉尽责,出具的审计报告存在虚假记载。深交所要求及时整改,杜绝再次发生。
尔康制药成立于2003年,于2011年上市,主要业务为医药产品的研发、生产和销售,主要产品有药用辅料及新型抗生素产品,曾获“全国医药上市公司前十强”等称号。2017年5月10日,由于媒体爆出尔康制药虚增收入,股票开始停牌。今年6月14日,尔康制药收到湖南证监局下发的《行政处罚决定书》。处罚决定书认定,2015年,尔康制药涉嫌虚增营业收入1805.88万元,虚增利润1586万元,占当期合并报表披露营业收入的1.03%,净利润的2.62%;2016年涉嫌虚增营业收入2.55亿元,虚增净利润2.32亿元,占当期合并报表披露营业收入的8.61%,净利润的22.63%。
对此,湖南证监局对尔康制药及相关高管进行了不同程度的处罚,其中对尔康制药责令改正,给予警告,并处以60万元顶格处罚罚款;对直接负责的主管人员给予警告,并分别处以30万元罚款;对其他责任人员分别处以3万-10万的罚款,并给予警告。
除业绩造假外,深交所还称,尔康制药2017半年度业绩预告披露的净利润与半年度报告存在重大差异,且业绩预告修正公告披露时间严重滞后。对于上述行为,深交所在今年11月3日对尔康制药给予公开谴责的处分,对公司董事长、总经理、财务总监给予公开谴责的处分,对副总经理、董秘等一众高管给予通报批评的处分。
受业绩造假一案影响,11月23日复牌即迎来4个跌停并持续下跌。股价从停牌前的11.41元降至8月21日3.25元的低点。11月7日,股价收于4.18元,跌0.24%。这让大股东的股票面临平仓风险:公司在8月18日披露,公司实控人帅放文持有公司股份已经有累计5.2亿股触及平仓线,占公司总股本比例为25.36%。帅放文目前持股8.5亿股,占总股本为41.44%,目前其质押股份7.2亿股,占其所持股份的84.7%。另据公司三季报,第二大股东湖南帅佳投资股份有限公司所持11.24%的股份被冻结, 帅放文持有帅佳投资5.9%股权。
除了行政处罚,尔康制药还面临着投资者的高额索赔。据公司公告显示,截止2018年10月12日,全国有481位投资者起诉尔康制药,索赔总额约29353万元。
2. 医械厂商宝莱特获国资股东驰援,但业绩困境依旧难解
11月5日晚,来自珠海的医疗器械上市公司宝莱特(300246.SZ)发布公告称,公司实控人燕金元与珠海华发集团有限公司(下称“华发集团”)签署协议,后者拟受让燕金元持有的公司730.44万股至1168.70万股股份(占公司股本的5%至8%),从而成为公司的战略股东。
燕金元目前持有宝莱特近4898万股股份,占公司总股本的33.53%,系公司控股股东,并担任董事长兼总裁。根据协议,华发集团拟采取现金收购的方式,在满足先决条件后以不高于12.80元/股的对价进行受让。按最高价格计算,华发集团需要支付的金额约为0.93亿元至1.50亿元。转让完成后,燕金元的持股比例将降至25.54%至28.54%左右,仍能保持对公司的控股与支配地位。
值得注意的是,根据公司披露的公告信息,自去年10月至今燕金元已累计补充质押6次,今年8月和9月就补充质押了4次,目前已累计质押3619万股股份,占其持有公司股份总数的73.89%,只剩1279万股尚未质押。自2016年8月以来,公司股价持续处于下降通道,今年以来累计跌幅超过40%,这也使得燕金元不断补充质押以解除平仓风险。宝莱特不断走低的股价导致实控人质押平仓风险持续堆积。目前燕金元尚未质押的股份高于此次计划转让股份的上限,故此次交易并不存在障碍,但是转让完成后,燕金元补充质押的空间将会明显受限,若股价难有起色,爆仓风险则会迎面而来。
从双方经营主业来看,宝莱特是一家从事医疗器械研产销的高新技术企业,业务涵盖健康监测和肾科医疗两大板块,产品以血透产品和监护仪产品为主。而本次计划引入的战略股东华发集团系珠海市国资委全资持股的两家龙头国企之一(另一家为格力集团),也是珠海最大的综合型企业集团,主要以城市运营、房产开发、金融产业、产业投资为四大核心业务。华发集团目前正计划借助产业投资进军高端制造业、大健康产业和高科技产业,与宝莱特存在一定的契合之处。
不过,宝莱特的业绩表现并不突出,上市七年后公司盈利规模仍旧在5000万元徘徊,且面临增长压力。今年公司依旧增收不增利,前三季度实现收入约5.97亿元,同比增长15%;净利润约0.50亿元,同比下降11%,去年同比降幅达14%。同时,宝莱特的盈利能力也不断降低。今年前三季度公司毛利率约为36.87%,相较于公司上市的2011年下降近11个百分点,其中占公司收入70%的血透产品的毛利率下降幅度同样惊人,今年上半年该产品毛利率为33.78%,相较于2012年已经下降近9个百分点。
针对业绩和盈利能力疲软的数据,宝莱特解释称主要系血透产品的原材料冰醋酸一直处于涨价趋势,且涨幅很大,导致血透产品的毛利率不断走低所致。根据Wind数据,冰醋酸的主要厂家上海吴泾、天津碱厂、山东兖矿以及华鲁恒升的出厂价自2016年以来均持续大幅度上涨,基本上都从2016年初期的2000元/吨左右上涨至近期的5000元/吨以上,甚至达到5600元/吨。市场观点认为,这主要受国外(印度)生产装置停产带动国内出口增加影响,以及环保因素导致。
尽管行业和企业自身均不占优势,但国资的引入依旧挑动了二级市场投资者的触角,11月6日宝莱特以涨停开盘,随后有所回落,当日收于12.20元每股,涨4.81%。
3. 智飞生物:HPV疫苗供不应求,与默沙东签署三年180亿采购大单
11月5日晚,智飞生物(300122.SZ)发布公告称,公司与默沙东的关联公司美国默沙东药厂有限公司签署了人类乳头瘤病毒(HPV)疫苗相关协议,进一步调整和确定了公司所代理的HPV疫苗的综合基础采购额,调整后的2019-2021年的采购总额为180.02亿元。
简评:智飞生物是默沙东四价和九价HPV疫苗在国内的独家代理商,这两个产品分别在去年11月和今年5月获得批签发证明并开始销售,并呈现出供不应求的局面,显示市场需求庞大。此次采购金额猛增至180多亿元,意味着未来三年默沙东将向国内大幅增加供应量,但可能会受到产能限制。对公司来说,HPV疫苗已成为公司盈利的重要增长点,随着采购额的大增和市场需求的增长有望贡献更多的业绩。
4.本周药企产品研发申报、审评审批进展情况
新药注册进展:本周有康恩贝(600572.SH)、海思科(002653.SZ)和华海药业(600521.SH)共3家公司披露了新药获批注册的消息,见下表:

新药研发进展:本周有康弘药业(002773.SZ)、健康元(600380.SZ)、丽珠集团(000513.SZ)、珍宝岛(603567.SH)共4家公司披露了新药获批注册的消息,见下表:
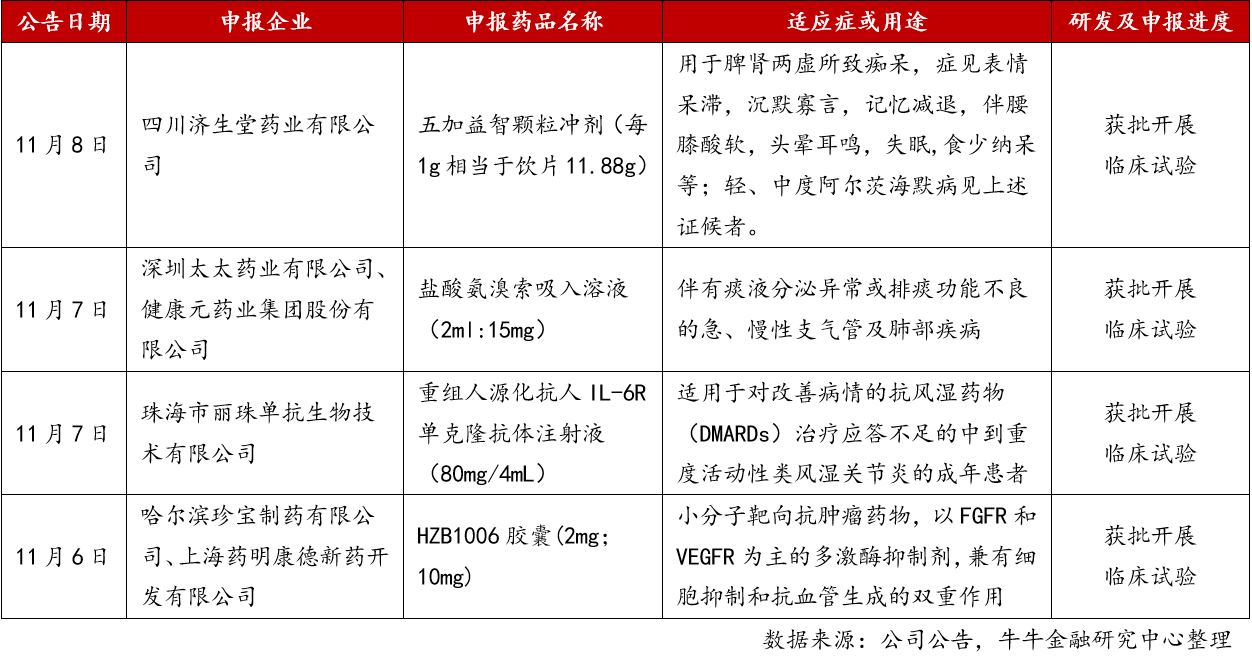
值得注意的是,其中丽珠集团申报的产品重组人源化抗人IL-6R单克隆抗体注射液属于罗氏原研药托珠单抗的生物类似药,国内本土药企尚无推出同类竞品;而珍宝岛申报的HZB1006胶囊则是公司和上海药明康德新药开发有限公司共同研发的1类创新抗癌药,已经累计研发投入约2700万元。
(文章来源:牛牛金融研究中心 刘景烨)
相关阅读
- 北京车展必看,25 万左右 SUV 人气排行榜,XC70 诚意出圈
- 赛力斯张正萍:问界秉承“五高”标准打造高端车
- 菜百股份2025年年报:营收净利双增 激活高质量发展新动能
- 华塑控股践行ESG发展理念,“精密制造+瓦斯治理”双轮驱动,经营质量持续向好
- 赛力斯一季度营利双增 研发费用增长70.7%加码技术护城河
- 数千万投入线下备考服务:高途考研梦中心背后的赛道升级逻辑
- 2026 国内 MES 系统排名:权威榜单、行业数据与推荐厂商发布
- 乐其创新SmallRig接待深圳市社会组织总会一行,共话产业协同与创新
- 技术体系完整性评分:从源头发现到市场转化的闭环
- 东鹏饮料:2026年一季报春节消费催热多元品类 拳头产品持续放量
推荐阅读
快讯 更多
- 01-28 11:21 | 启佑志愿重磅升级:首创“就业导向型”志愿填报新模式,破解升学与就业脱节难题
- 07-09 13:16 | 三重焕新,启航未来——Pivotal中文品牌发布暨乔迁新址、新官网上线
- 04-10 11:21 | 为“首发经济”注入创新动力,CMEF见证宽腾医学影像技术革新
- 02-20 18:53 | 手机也要上HBM芯片?三星计划推出移动版HBM,预计首款产品2028年上市
- 12-30 16:40 | 国产首款DDR5内存问世!价格战开启,复制长江存储击败三星路径!
- 12-30 16:36 | 华为手机回归第一年:全年销量或超4000万台 有望凭借Mate 70在高端市场击败苹果
- 11-26 18:19 | 众兴菌业拟与涟水县人民政府签订《招商引资合同书》 拟投资设立涟水食用菌产业园项目
- 11-26 18:16 | 美芝股份中选vivo全球AI研发中心-精装工程采购项目(标段二)
- 11-26 18:14 | 健之佳拟用不超1亿回购公司股份 维护公司价值及股东权益
- 11-26 09:53 | 格灵深瞳收购深圳市国科亿道科技有限公司部分股权并增资5000万




